Периодическая таблица химических элементов Д.И.Менделеева
В природе существует очень много повторяющихся последовательностей:
- времена года;
- время суток;
- дни недели…
В середине 19 века Д.И.Менделеев заметил, что химические свойства элементов также имеют определенную последовательность (говорят, что эта идея пришла ему во сне). Итогом чудесных сновидений ученого стала Периодическая таблица химических элементов, в которой Д.И. Менделеев выстроил химические элементы по возрастанию атомной массы. В современной таблице химические элементы выстроены по возрастанию атомного номера элемента (количество протонов в ядре атома).
Атомный номер изображен над символом химического элемента, под символом - его атомная масса (сумма протонов и нейтронов). Обратите внимание, что атомная масса у некоторых элементов является нецелым числом! Помните об изотопах! Атомная масса - это средневзвешенное от всех изотопов элемента, встречающихся в природе в естественных условиях.

Под таблицей расположены лантаноиды и актиноиды.
Металлы, неметаллы, металлоиды
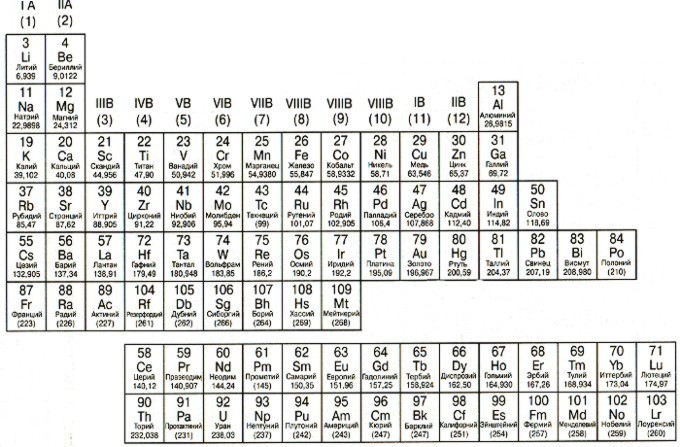
Расположены в Периодической таблице слева от ступенчатой диагональной линии, которая начинается с Бора (В) и заканчивается полонием (Po) (исключение составляют германий (Ge) и сурьма (Sb). Нетрудно заметить, что металлы занимают бОльшую часть Периодической таблицы. Основные свойства металлов: твердые (кроме ртути); блестят; хорошие электро- и теплопроводники; пластичные; ковкие; легко отдают электроны.
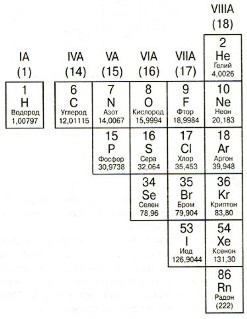
Элементы, расположенные справа от ступенчатой диагонали B-Po, называются неметаллами . Свойства неметаллов прямо противоположны свойствам металлов: плохие проводники тепла и электричества; хрупкие; нековкие; непластичные; обычно принимают электроны.
Металлоиды
Между металлами и неметаллами находятся полуметаллы (металлоиды). Для них характерны свойства как металлов, так и неметаллов. Основное применение в промышленности полуметаллы нашли в производстве полупроводников, без которых немыслима ни одна современная микросхема или микропроцессор.
Периоды и группы
Как уже говорилось выше, периодическая таблица состоит из семи периодов. В каждом периоде атомные номера элементов увеличиваются слева направо.
Свойства элементов в периодах изменяются последовательно: так натрий (Na) и магний (Mg), находящиеся в начале третьего периода, отдают электроны (Na отдает один электрон: 1s 2 2s 2 2p 6 3s 1 ; Mg отдает два электрона: 1s 2 2s 2 2p 6 3s 2). А вот хлор (Cl), расположенный в конце периода, принимает один элемент: 1s 2 2s 2 2p 6 3s 2 3p 5 .
В группах же, наоборот, все элементы обладают одинаковыми свойствами. Например, в группе IA(1) все элементы, начиная с лития (Li) и заканчивая францием (Fr), отдают один электрон. А все элементы группы VIIA(17), принимают один элемент.
Некоторые группы настолько важны, что получили особые названия. Эти группы рассмотрены ниже.
Группа IA(1) . Атомы элементов этой группы имеют во внешнем электронном слое всего по одному электрону, поэтому легко отдают один электрон.
Наиболее важные щелочные металлы - натрий (Na) и калий (K), поскольку играют важную роль в процессе жизнедеятельности человека и входят в состав солей.
Электронные конфигурации:
- Li - 1s 2 2s 1 ;
- Na - 1s 2 2s 2 2p 6 3s 1 ;
- K - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1
Группа IIA(2) . Атомы элементов этой группы имеют во внешнем электронном слое по два электрона, которые также отдают во время химических реакций. Наиболее важный элемент - кальций (Ca) - основа костей и зубов.
Электронные конфигурации:
- Be - 1s 2 2s 2 ;
- Mg - 1s 2 2s 2 2p 6 3s 2 ;
- Ca - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2
Группа VIIA(17) . Атомы элементов этой группы обычно получают по одному электрону, т.к. на внешнем электронном слое находится по пять элементов и до "полного комплекта" как раз не хватает одного электрона.
Наиболее известные элементы этой группы: хлор (Cl) - входит в состав соли и хлорной извести; йод (I) - элемент, играющий важную роль в деятельности щитовидной железы человека.
Электронная конфигурация:
- F - 1s 2 2s 2 2p 5 ;
- Cl - 1s 2 2s 2 2p 6 3s 2 3p 5 ;
- Br - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5
Группа VIII(18). Атомы элементов этой группы имеют полностью "укомплектованный" внешний электронный слой. Поэтому им "не надо" принимать электроны. И отдавать их они "не хотят". Отсюда - элементы этой группы очень "неохотно" вступают в химические реакции. Долгое время считалось, что они вообще не вступают в реакции (отсюда и название "инертный", т.е. "бездействующий"). Но химик Нейл Барлетт открыл, что некоторые из этих газов при определенных условиях все же могут вступать в реакции с другими элементами.
Электронные конфигурации:
- Ne - 1s 2 2s 2 2p 6 ;
- Ar - 1s 2 2s 2 2p 6 3s 2 3p 6 ;
- Kr - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6
Валентные элементы в группах
Нетрудно заметить, что внутри каждой группы элементы похожи друг на друга своими валентными электронами (электроны s и p-орбиталей, расположенных на внешнем энергетическом уровне).
У щелочных металлов - по 1 валентному электрону:
- Li - 1s 2 2s 1 ;
- Na - 1s 2 2s 2 2p 6 3s 1 ;
- K - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1
У щелочноземельных металлов - по 2 валентных электрона:
- Be - 1s 2 2s 2 ;
- Mg - 1s 2 2s 2 2p 6 3s 2 ;
- Ca - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2
У галогенов - по 7 валентных электронов:
- F - 1s 2 2s 2 2p 5 ;
- Cl - 1s 2 2s 2 2p 6 3s 2 3p 5 ;
- Br - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5
У инертных газов - по 8 валентных электронов:
- Ne - 1s 2 2s 2 2p 6 ;
- Ar - 1s 2 2s 2 2p 6 3s 2 3p 6 ;
- Kr - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6
Дополнительную информацию см. в статье Валентность и в Таблице электронных конфигураций атомов химических элементов по периодам .
Обратим теперь свое внимание на элементы, расположенные в группах с символов В . Они расположены в центре периодической таблицы и называются переходными металлами .
Отличительной особенностью этих элементов является присутствие в атомах электронов, заполняющих d-орбитали :
- Sc - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1 ;
- Ti - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2
Отдельно от основной таблицы расположены лантаноиды и актиноиды - это, так называемые, внутренние переходные металлы . В атомах этих элементов электроны заполняют f-орбитали :
- Ce - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 4d 10 5s 2 5p 6 4f 1 5d 1 6s 2 ;
- Th - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 4d 10 5s 2 5p 6 4f 14 5d 10 6s 2 6p 6 6d 2 7s 2